
|
|
라디오 전자 및 전기 공학의 백과사전 크기 AA의 갈바닉 요소의 비교 특성. 무선 전자 및 전기 공학 백과사전
무선 전자 및 전기 공학 백과사전 / 충전기, 배터리, 갈바니 전지 오늘날 상점과 시장에서 다양한 갈바닉 전지를 찾을 수 있습니다. 어떤 것을 선택해야 할까요? 이 기사는 올바른 결정을 내리는 데 도움이 될 것입니다. 갈바니 전지 및 배터리는 다양한 전자 장비에 전원을 공급하는 데 널리 사용됩니다. AA 크기 요소가 가장 널리 사용됩니다. 선반에서 다른 회사의 유사한 제품, 주로 식염수와 알칼리성의 두 가지 전기 화학 시스템을 찾을 수 있습니다. 최근에 Energizer는 1,5V AA 리튬 배터리를 출시했습니다. 갈바니 전지의 가장 중요한 특성인 용량(부하에 공급할 수 있는 전기량)은 라벨에 거의 표시되지 않습니다. 구매자는 "기존 소금보다 최대 2배 더 오래 작동하는" 전지에 대한 텔레비전 광고에 집중하거나 새로운 AA 리튬 e1 전지가 기존 알카라인 전지보다 XNUMX배 더 오래 지속된다고 주장하는 Energizer의 말을 받아들여야 합니다[XNUMX ]. 더욱이 어떤 요소가 "일반"이라고 불리는지는 완전히 명확하지 않습니다. 서로 다른 전기화학적 시스템의 원소 파라미터를 정량적으로 비교하기 위해서는 동일한 조건에서 테스트가 필요하다. 이러한 테스트는 소금 Philips Long Life("신선한" 셀의 emf - 1,65V), 알칼리성 Duracell Ultra M1,62(2V) 및 리튬 에너자이저 e1,8(15V)의 세 가지 유형의 셀로 수행되었습니다. 그들 각각은 약 100mA의 초기 방전 전류에 해당하는 1옴 저항으로 로드되었습니다. 크기 AA 요소의 경우 이러한 부하 전류가 일반적입니다. 방전은 실제 작동 조건에 해당하는 하루 수 시간 주기로 수행되었습니다. 이것은 Fig. XNUMX. 파란색 곡선은 소금 원소, 빨간색은 알칼리성, 녹색은 리튬에 해당합니다. "휴식" 중에는 모든 유형의 요소에 대한 전압이 약간 증가했지만 부하가 연결된 후에는 이전 사이클에서 최소값으로 빠르게 감소했습니다. 점은 요소의 EMF 값, 즉 부하가 없는 전압을 표시합니다.
셀의 완전 방전에 대한 기준으로 부하에서 전압이 0,9V로 감소하면 실험적으로 결정된 소금 셀의 용량은 1Ah, 알칼리 셀은 2,9Ah, 리튬 셀은 3,5A입니다. 아. 결과적으로 서로 다른 전기화학적 시스템의 요소 정전 용량의 XNUMX배 또는 XNUMX배 차이에 대해 말할 필요가 없습니다. 무화과에. 2는 다른 일련의 곡선을 보여줍니다.
방전 과정에서 요소의 내부 저항이 어떻게 변했는지 보여줍니다. 요소 유형과 곡선 색상 간의 대응 관계는 그림과 동일합니다. 1. 내부 저항 R의 값은 다음 공식으로 계산되었습니다.
여기서 E는 요소의 EMF입니다. U - 부하 전압; RH는 부하 저항입니다. 염 및 알칼리 원소의 내부 저항은 방전될 때 단조롭게 증가합니다. 그리고 방전 초기에 급격히 감소한 리튬의 저항은 끝까지 거의 변하지 않고 급격히 증가합니다. 물론 수행 된 실험을 철저하다고 할 수는 없습니다. 요소의 용량은 엄격하게 고정된 값이 아니라 많은 외부 요인에 따라 달라집니다. 서로 다른 요소의 경우 상당히 다른 방전 조건에서 최대값을 얻을 수 있습니다. 이 모든 것을 고려하려면 아마추어 조건에서는 비현실적인 매우 큰 일련의 실험을 수행해야 합니다. 그러나 얻은 결과를 계산으로 확인해보자. 다양한 전기화학적 시스템의 소자의 최대 가능 용량을 이론적으로 추정하기 위해서는 전극, 전해질의 화학적 조성 및 소자에서 일어나는 화학 반응을 알아야 합니다. 식염수 및 알칼리 전지에서 음극은 아연이고 양극은 이산화망간입니다. 이러한 이유로 이러한 원소를 총칭하여 망간-아연이라고 합니다. 그러나 그것들의 전해질은 다릅니다 : 소금 (일반적으로 염화 암모늄) 또는 알칼리 (수산화 칼륨). [2]에 따르면, 염 망간-아연 원소에서 반응이 일어난다.
그리고 알칼리성
전극의 재료와 리튬 전지의 화학 반응에 대한 신뢰할 수 있는 정보가 없습니다. 전극은 리튬과 이산화망간이고 전해질은 프로필렌 카보네이트에 과염소산 리튬 용액이라고 가정할 수 있습니다. 이 추측이 맞다면 [2]에 따라 리튬 전지는 다음과 같은 반응을 겪는다.
패러데이의 법칙을 사용하여 갈바니 전지 C, Ah의 커패시턴스를 결정하는 식을 얻습니다.
여기서 m은 반응 물질의 질량 F = 96,5-103 C/g-eq는 패러데이 수입니다. n - 원자가(염 및 알칼리성 갈바니 전지의 경우 - 2, 리튬의 경우 - 1); M은 반응물의 총 분자량입니다. 우리는 AA 크기의 갈바니 전지의 무게를 잰다: 소금 - 17g, 알칼리성 - 24g, 리튬 - 15g. )는 무시할 만하고 무시할 수 있습니다. 우리는 위의 화학 반응 방정식에서 반응 물질의 총 분자량을 계산합니다 : 소금 - 346g, 알칼리성 - 257g, 리튬 - 94g 공식에 수치를 대입하면 가능한 최대 값을 얻습니다. 염 원소의 용량 - 2,6 Ah , 알칼리성 - 5 Ah, 리튬 - 4,3 Ah. 계산된 커패시턴스 값과 측정된 값의 차이는 계산에서 이루어진 대략적인 가정으로 설명할 수 있습니다. 따라서 XNUMX배와 XNUMX배의 차이는 발견되지 않았습니다. 알카라인 전지의 이론적 용량은 염전지의 약 XNUMX배이며 리튬은 이 점에서 알칼리 전지에 비해 이점이 없습니다. 이는 실험 결과와 일치합니다. 완료된 모든 작업의 결과를 바탕으로 다음과 같은 결론을 내릴 수 있습니다. 1. 리튬 갈바닉 셀은 전압이 가장 안정적이고 내부 저항이 가장 낮아 방전 정도에 거의 영향을 받지 않으며 용량은 크지 않지만 가장 큽니다. 전원 전압이 떨어지면 자동으로 꺼지는 장치(예: 디지털 카메라)뿐만 아니라 소비 전류가 큰 장치에 전원을 공급하는 데 사용하는 것이 좋습니다. 2. 알카라인 전지는 리튬에 필적하는 용량을 가지며 부하에 높은 전류를 전달할 수 있지만 전압은 낮습니다. 자동 전압 제어가 없는 평균 전류 소비 장치에 가장 적합합니다. 많은 경우에 알카라인 전지가 리튬보다 XNUMX~XNUMX배 더 저렴하기 때문에 선호됩니다. 3. 염전지는 정전 용량이 가장 작고 내부 저항이 가장 큽니다. 전류 소모가 적은 장비에 사용하는 것이 좋습니다. 문학
저자: I.Podushkin, 모스크바
터치 에뮬레이션을 위한 인조 가죽
15.04.2024 펫구구 글로벌 고양이 모래
15.04.2024 배려심 많은 남자의 매력
14.04.2024
▪ Mean Well PSC-160 보안 전원 공급 장치 ▪ 미생물 복원제
▪ 기사 그리고 모든 곳에서 치명적인 열정이 있으며 운명으로부터 보호받지 못합니다. 대중적인 표현 ▪ 기사 왜 미국인들은 Pindos라고 불립니까? 자세한 답변 ▪ 기사 부품의 하이드로 샌드 블라스트 세척 중 금속 코팅 적용. 노동 보호에 관한 표준 지침 ▪ DIY IrDA 기사. 무선 전자 및 전기 공학 백과사전 ▪ 기사 RA3AAE 트랜시버의 현대화. 무선 전자 및 전기 공학 백과사전 기사에 대한 의견: 손님 설명글, 감사합니다.
홈페이지 | 도서관 | 조항 | 사이트 맵 | 사이트 리뷰 www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese






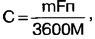
 이 기사에 대한 의견을 남겨주세요:
이 기사에 대한 의견을 남겨주세요: